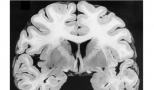
Ювенильная макулярная дегенерация (болезнь Штаргардта). Характерные признаки и последствия абиотрофии сетчатки и её профилактика Штаргардта болезнь лечение за рубежом
Возникает дистрофия Штаргардта в результате передачи патологического гена, который кодирует синтез белка-переносчика АТФ к светочувствительным клеткам сетчатки. Из-за недостатка энергии эти образования отмирают с форсированием темного пятна на поле зрения или неправильного восприятия цветовой гаммы, а также формы окружающих предметов. Лечение заключается в проведении поддерживающей терапии с замедлением прогрессирования симптоматики.
Болезнь проявляется преимущественно в детском или подростковом возрасте.
Этиология
Болезнь Штаргардта является наследственной патологией и передается по аутосомно-доминантному или рецессивному типу. Возникновение дистрофии сетчатки не зависит от пола. При этом происходит нарушение синтеза белка, который участвует в транспорте АТФ к макулярной зоне. Это явление провоцирует отмирание и нарушение функциональной активности светочувствительных клеток, что вызвано недостатком транспорта к ним энергии из сосудистой оболочки. Также осуществляется скопление белка транс-ретиналя, который превращается в липофусцин, что оказывает токсическое действие на сетчатку. Протеин является продуктом распада родопсина и в процессе прогрессирования болезни нарушается его восстановление. При доминантной разновидности наследования болезнь протекает намного легче.
Разновидности
 При центральном типе патологии пятно закрывает объект, на который направлен взгляд.
При центральном типе патологии пятно закрывает объект, на который направлен взгляд.
Дегенерация Штаргардта в зависимости от локализации очага патологического процесса на сетчатке бывает таких видов:
- Центральная. Проявляется выпадением основной зоны поля зрения и появлением скотомы в точке фиксации взгляда.
- Периферическая. Характеризуется возникновением темного пятна сбоку от точки фокусировки взгляда.
- Смешанная.
Основные симптомы
Синдром Штаргардта характеризуется возникновением у пациента таких клинических признаков:
- плохое видение черно-белых предметов;
- поражение обоих глаз;
- нарушение и неправильное восприятие цветов;
- появление центральной или периферической скотомы;
- полная слепота, вызванная атрофией зрительного нерва.
Способы диагностики
 Для проверки правильности диагноза доктор проводит офтальмоскопию.
Для проверки правильности диагноза доктор проводит офтальмоскопию. Выявить, что у пациента макулодистрофия Штаргардта, можно по наличию характерных для этой патологии клинических признаков. Для подтверждения диагноза рекомендуется провести офтальмоскопию, где обнаруживается кольцо на сетчатке с пониженной пигментацией. Также на желтом пятне определяются патологические включения. При выявлении цветовосприятия наблюдается красно-зеленая дейтеранопия, когда один цвет видится больным как совершенно другой. Электрография показывает снижение передачи нервных импульсов. Также рекомендуется выполнить флуоресцентную ангиографию, где выявляется темная сосудистая оболочка. Выполняют биопсию участка макулы с последующим гистологическим исследованием. Диагноз подтверждается при накоплении в биоптате большого количества липофусцина. Окончательная постановка диагноза выполняется после молекулярно-генетического анализа и обнаружения дефектного гена.
Ювенильной макулярной дегенерацией или болезнью Штаргардта называют один из видов наследственной дистрофии макулярной области сетчатки. Заболевание выявляется в 12-20 летнем возрасте и проявляется прогрессирующим снижением остроты зрения обоих глаз.
В зависимости от местоположения патологии, принято выделять 4 формы ювенильной макулярной дегенерации:
- В области макулы;
- На средней периферии;
- В парацентральной области;
- В центральной и периферийной областях (смешанная форма).
Проводимые в настоящее время генетические исследования, доказывают, что ювенильная макулярная дегенерация и болезни Франческетти (жёлтопятнистое глазное дно), это фенотипические признаки одного заболевания.
Причины возникновения
Заболевание передается аутосомно-рецессивным путем наследования, редко аутосомно-доминантным. Посредством позиционного клонирования для ювенильной макулярной дегенерации определен основной локус вызывающего заболевание гена. Он экспрессируется в фоторецепторах и носит название АВСR. ABCR - это член суперсемейства т.н. АТФ-связывающего кассетного транспортёра, идентичный по последовательности человеческому гену RmP.
При аутосомно-доминантном пути наследования болезни, определена локализация генов мутации в хромосомах 13q, а также 6q14. Выявлено, что мутации ABCR присутствуют в субпопуляции больных с неэкссудативной формой макулодистрофии, связанной с возрастом и колбочко-палочковой дегенерацией, что позволяет предположить генетически обусловленный риск развития АМД у кровных родственников больных.
Видео нашего специалиста о заболевании
Симптомы заболевания
В пигментном эпителии сетчатой оболочки глаза возникает интенсивное накопление липофусцина. Процесс сопровождается ослаблением окислительной функции лизосом, с увеличением pH в клетках пигментного эпителия, что приводит к изменению их мембранной целостности.
При центральной форме ювенильной дистрофии, по мере развития заболевания, офтальмоскопическая картина области макулы имеет следующий вид: «битого металла», далее «бычьего глаза», затем «кованой бронзы» и в последствие - атрофии хороидеи.
Офтальмоскопия на стадии феномена «бычий глаз», выявляет тёмный центр, который окружён широким кольцом гипопигментации и, следующим за ним, еще одним кольцом гиперпигментации. Сосуды сетчатки - без изменений, ДЗН с темпоральной стороны бледен, что обусловлено атрофией нервных волокон папилломакулярного пучка. Фовеолярный рефлекс отсутствует, как и макулярное возвышение.
Наличие пятен желтовато-белого цвета, обнаруживается в ретинальном пигментном эпителии заднего полюса глаза. Пятна имеют различную величину, форму и конфигурацию — это наиболее характерный симптом желто-пятнистого глазного дна. Со временем форма, цвет и размеры пятен могут изменяться. Желтоватые первоначально пятна, с четко очерченными краями, спустя несколько лет нередко становятся серыми, границы их смазываются или исчезают.

Диагностика заболевания
В процессе сбора анамнеза, выясняется время возникновения заболевания (возраст манифестации), что играет важную роль в диагностике.
При лабораторных гистологических исследованиях в центральной области глазного дна отмечают увеличение пигмента, атрофию прилегающего пигментного эпителия сетчатки, комбинированную атрофию и гипертрофию пигментного эпителия. Представление желтых пятен липофусциноподобным материалом.
В ходе инструментальных исследований, при периметрии у пациентов с ювенильной макулярной дегенерацией обнаруживают разной величины относительные либо абсолютные центральные скотомы, что зависит от сроков процесса и его распространенности - с раннего детства или юношеского возраста. В случае желто-пятнистого глазного дна, изменений в области макулы не отмечается, поле зрения, зачастую, не изменено.
Цветоаномалии у большинства больных с центральной локализацией паталогического процесса развиваются по типу дейтеранопии или красно-зелёной дисхромазии, нередко более выраженной.
Цветовое зрение в случае желто-пятнистого глазного дна может не изменяться. Пространственная контрастная чувствительность значительно изменена во всех диапазонах пространственных частот, значительно снижена в зоне средних и полностью отсутствует в зоне высоких пространственных частот (т.н. паттерн-колбочковая дистрофия). Контрастная чувствительность отсутствует в центральной зоне сетчатки в границах 6-10 градусов.
Острота зрения, поле зрения и цветовое зрение находятся в норме. Темновая адаптация, как правило нормальная или незначительно снижена.
На ФАГ, в случае типичного феномена «бычьего глаза», при нормальном фоне выявляются зоны «отсутствия» или в ряде случаев гинофлюоресценции, с присутствием видимых хориокапилляров, а также «тёмная» или «молчащая» хороидея. Отсутствие в макулярной области флюоресценции объяснимо накоплением липофусцина, который экранирует флуоресцеин. Участки с гипофлюоресценцией иногда становятся гиперфлюоресцирующими в соответствии с зонами атрофии пигментно-эпителиального слоя.
Дифференциальная диагностика
Диагностику серьезно затрудняет сходство клинической картины многих дистрофических заболеваний в области макулы. Дифференциальный диагноз ювенильной макулярной дистрофии проводят с семейными друзами, пятнами сетчатки Кандори, прогрессирующей доминантной фовеальной дистрофией; ювенильным ретиношизисом; колбочковой, колбочко-палочковой, палочко-колбочковой дистрофиями; вителлиформной макулярной дистрофией; лекарственными дистрофиями.
Лечение и прогноз
Патогенетически обоснованного лечения ювенильной макулярной дегенерации до сегодняшнего дня нет. Необходимо постоянное наблюдение специалиста, контроль поля зрения, мониторинг ЭРГ, ЭОГ.
ОПРЕДЕЛЕНИЕ
Болезнь Штаргардта - дистрофия макулярной области сетчатки, которая начинается в ПЭС и манифестирует двусторонним снижением остроты зрения в возрасте 10-20 лет.
КОД ПО МКБ-10
Н35.5 Наследственные ретинальные дистрофии.
КЛАССИФИКАЦИЯ
Выделяют четыре формы болезни Штаргардта в зависимости от локализации патологического процесса: в макулярной области, на средней периферии (fundus flavimaculatus), в парацентральной области, а также смешанную форму при локализации в центре и на периферии.
ЭТИОЛОГИЯ
В настоящее время с помощью генетических исследований доказано, что болезнь Штаргардта и жёлто-пятнистое глазное дно - фенотипические проявления одного и того же заболевания с аутосомно-рецессивной, редко аутосомно-доминантной формой наследования.
Позиционным клонированием определён основной локус гена АВСR для болезни Штаргардта, экспрессирующегося в фоторецепторах. ABCR-член суперсемейства АТФ-связывающего кассетного транспортёра. При аутосомно-доминантном типе наследования болезни Штаргардта определена локализация мутированных генов на хромосомах 13q и 6q14; анализ связи при картировании локуса для центральной и периферической формах болезни Штаргардта.
ПАТОГЕНЕЗ
В ПЭС происходит интенсивное накопление липофусцина. Он ослабляет окислительную функцию лизосом, увеличивает pH клеток ПЭС, что приводит к нарушению из мембранной целостности.
КЛИНИЧЕСКАЯ КАРТИНА
При центральной форме дистрофии Штаргардта по мере развития процесса офтальмоскопическая картина макулярной области имеет различный вид: от "битого металла" до «бычьего глаза», «кованой бронзы» и атрофии хороидеи.
Феномен «бычий глаз» офтальмоскопически виден как тёмный центр, окружённый широким кольцом гипопигментации, за которым обычно следует другое кольцо гиперпигментации. Сосуды сетчатки не изменены, ДЗН бледен с темпоральной стороны, что связано с атрофией нервных волокон в папилломакулярном пучке. Фовеолярный рефлекс и макулярное возвышение (umbo) отсутствуют.
Наличие желтовато-белых пятен в заднем полюсе глаза в ретинальном пигментном эпителии различной величины, формы и конфигурации - характерный признак жёлто-пятнистого глазного дна (fundus flavimaculatus). Со временем цвет, форма, размеры этих пятен могут изменяться. Первоначально желтоватые пятна с чётко очерченными краями через несколько лет могут стать серыми с нечёткими границами или исчезнуть.
ДИАГНОСТИКА
Анамнез
Время возникновения заболевания (в детском или юношеском возрасте) может играть важную роль в его диагностике.
Лабораторные исследования
Гистологически отмечают увеличение количества пигмента в центральной зоне глазного дна, атрофию прилежащего ПЭС, комбинацию атрофии и гипертрофии пигментного эпителия. Жёлтые пятна представлены липофусциноподобным материалом.
Инструментальные исследования
При периметрии у всех больных с болезнью Штаргардта обнаруживают относительные или абсолютные центральные скотомы разной величины в зависимости от сроков и распространения процесса с раннего детского или юношеского возраста. При жёлто-пятнистом глазном дне изменений в макулярной области не отмечают, поле зрения может быть не изменено.
Форма цветоаномалии у большинства пациентов с центральной локализацией процесса - по типу дейтеранопии, красно-зелёной дисхромазии или более выраженной.
При жёлто-пятнистом глазном дне цветовое зрение может быть не изменено. Пространственная контрастная чувствительность при дистрофии Штаргардта значительно изменена во всём диапазоне пространственных частот со значительным снижением в области средних и полным её отсутствием в области высоких пространственных частот - "паттерн-колбочковой дистрофии". Контрастная чувствительность (on- и off-активность колбочковой системы) отсутствует в центральной области сетчатки в пределах 6-10 градусов.
ЭРГ и ЭОГ. Макулярная ЭРГ снижается уже в начальных стадиях центральной формы дистрофии Штаргардта и не регистрируется в развитых стадиях.
В начальных стадиях fundus flavimaculatus ганцфельд ЭРГ и ЭОГ остаются в пределах нормы: в развитых стадиях снижаются колбочковые и палочковые компоненты ЭРГ, которая становится субнормальной, так же изменяются показатели ЭОГ. У больных при этой форме симптомы отсутствуют. Острота зрения, цветовое зрение, поле зрения находятся в пределах нормы. Темновая адаптация может быть нормальной или незначительно сниженной.
На ФАГ при типичном феномене «бычьего глаза» на нормальном фоне обнаруживают зоны «отсутствия», или гинофлюоресценции, с видимыми хориокапиллярами, «тёмную», или «молчащую», хороидею. Отсутствие флюоресценции в макулярной области объясняют накоплением липофусцина, экранирующего флуоресцеина. Участки с гипофлюоресценцией могут становиться гиперфлюоресцирующими, что соответствует зоне атрофии ПЭС.
Дифференциальная диагностика
Сходство клинической картины различных дистрофических заболеваний макулярной области затрудняет диагностику. Дифференциальный диагноз болезни Штаргардта следует проводить с семейными друзами, fundus albipunctatus, пятнами сетчатки Кандори, доминантной прогрессирующей фовеальной дистрофией, колбочковой, колбочко-палочковой и палочко-колбочковой дистрофией, ювенильным ретиношизисом, вителлиформной макулярной дистрофией, приобретёнными лекарственными дистрофиями (например, хлороквиновой ретинопатией).
Болезнь Штаргардта (ювенильная макулярная дегенерация, желтопятнистая абиотрофия сетчатки) – это юношеская форма центральной дегенерации сетчатки, для которой характерно прогрессирующее поражение макулярной области. Болезнь имеет преимущественно аутосомно-доминантный, реже – аутосомно-рецессивный или сцепленный с полом механизм наследования. Патология встречается с частотой 1:10000 и проявляется в возрасте от 6 до 20 лет.
Впервые заболевание было описано немецким офтальмологом Карлом Штаргардтом еще вначале XX века. В 1997 году генетиками был обнаружен дефект гена ABCR, обусловливающий нарушение синтеза белка, который переносит АТФ к фоторецепторам сетчатки. Именно дефицит энергии приводит к гибели разных типов колбочек в области макулы. Следует отметить, что желтопятнистая абиотрофия сетчатки может возникать при мутации CRB1, RP2 и еще около 150 других генов.
Классификация
Выделяют два основные типа болезни Штаргардта: с fundus flavimaculatus и без него.
Для первого характерно наличие типичных изменений, имеющих вид желто-белых полос и точек, для второго – их отсутствие.
 В зависимости от локализации бывают такие формы болезни:
В зависимости от локализации бывают такие формы болезни:
- центральная;
- перицентральная;
- центропериферическая (смешанная).
Учитывая характер изменений на глазном дне, выделяют следующие типы патологии:
- дегенеративные изменения в макуле без крапчастости;
- макулярная дегенерация с парафовеальной крапчастостью;
- дегенерация с диффузной крапчастостью;
- диффузная крапчастость без дегенеративных изменений в макулярной области.
Симптомы
Первые проявления болезни обычно возникают в возрасте 6-7 лет. Для ювенильной макулярной дегенерации характерно симметричное поражение обоих глаз. Все дети с данной патологией отмечают появление абсолютных или относительных скотом – черных или цветных пятен в поле зрения. Локализация скотомы напрямую зависит от расположения патологического очага.

Для центральной формы ювенильной макулярной дегенерации характерно выпадение поля зрения в самой точке фиксации. При парацентральной форме скотомы появляются в стороне от точки фиксации. Они могут иметь вид полумесяца или черного кольца. Для центропериферической формы болезни характерен быстрый рост скотомы, из-за чего она может закрывать большую часть поля зрения.
У некоторых больных обнаруживают дейтеранопию, красно-зеленую дихромазию и другие, не поддающиеся классификации, нарушения цветового зрения. Многие дети жалуются на светобоязнь и прогрессирующее снижение остроты зрения.
У малышей нередко выявляют нарушение темновой адаптации и снижение контрастной чувствительности.
Методы диагностики
Для заболевания характерны полиморфные изменения, однако, у больных практически всегда выявляют участки депигментации и пигментированные округлые точки. При офтальмоскопии на глазном дне видны характерные изменения в виде бычьего глаза, следа улитки, битой (кованой) бронзы, атрофии хориоидеи, географической атрофии.

Помимо стандартного офтальмологического обследования лицам с болезнью Штаргардта назначают электрофизиологические методы исследования. Наиболее информативными являются электроретинография (ЭРГ) и электроокулография (ЭОГ). Эти методы позволяют оценить функциональное состояние сетчатой оболочки глаза.
На видео врач рассказывает о причинах, симптомах и лечении заболевания:
Лечение
На сегодняшний день этиологического лечения болезни нет.
В качестве вспомогательной терапии больному могут назначаться физиотерапевтические процедуры, витамины, антиоксиданты, таурин, сосудорасширяющие средства, стероидные гормоны.
Болезнь Штаргардта, являющаяся классическим примером центральной пигментной дегенерации, была описана К. Stargardt (1909, 1913) еще в начале XX в. как наследственное заболевание макулярной области, проявляющееся в детском и молодом возрасте (7-20 лет). Изменения на глазном дне, хотя и полиморфны, характеризуются появлением в обоих глазах пигментированных круглых точек, участков депигментации и атрофии ретинального пигментного эпителия (РПЭ), в ряде случаев типа "бычий глаз", сочетающихся часто с беловато-желтоватыми пятнами в парамакулярной зоне. Подобная клиническая картина прогрессирующей дегенерации макулярной области сетчатки у детей была описана еще в XIX в..
Изменения в виде желтовато-беловатых точек и полос с изменениями в макулярной области или без них A. Franceschetti обозначил термином "fundus flavimaculatus". В литературе термины "болезнь Штаргардта" и "фундус флавимакулятус" нередко объединяют (Stargardt disease/fundus flavimaculatus), подчеркивая тем самым предполагаемое единство происхождения и/или переход из одной формы заболевания (болезнь Штаргардта) в другую (фундусс флавимакулятус) по мере ее развития.
Если снижение зрения, обусловленное типичными дистрофическими изменениями желтого пятна, начинается в первые две декады жизни, то предпочтительнее употреблять термин "болезнь Штаргардта". Если же изменения появляются в центральных и периферических отделах сетчатки в более позднем возрасте и заболевание острее прогрессирует, то рекомендуется использовать термин "фундус флавимакулатус".
 Установлено, что это гетерогенная группа заболеваний с наследственной передачей.
Установлено, что это гетерогенная группа заболеваний с наследственной передачей.
Симптомы (в порядке появления):
- В фовеа - без изменений или с перераспределением пигмента
- Овальные очаги типа "следа улитки" или бронзовый рефлекс, который может быть окружен бело-желтыми пятнами.
- "Географическая" атрофия, может иметь вид "бычьего глаза".
Классификация
Наряду с классическим выделением двух типов болезни Штадгардта, включающих дистрофию макулярной области с и без фундус флавимакулатус, редложено несколько других классификаций, основанных на вариациях клинической картины глазного дна.
Так, K.G. Noble и R.E. Саrr (1971) выделили четыре типа заболеваний:
- I тип - макулярная дегенерация без пятен (крапчатости). Острота зрения снижается рано.
- II - с парафовеальной крапчатостью,
- III - макулярная дегенерация с диффузной крапчатостью,
- IV тип - диффузная крапчатость без макулярной дегенерации. Острота зрения остается достаточно высокой, поскольку поражение сетчатки не затрагивает фовеальную область.
Генетические исследования
Дистрофия Штаргардта наиболее часто наследуется по аутосомно-рецессивному типу, однако описано много семейств, в которых передача болезни осуществляется аутосомно-доминантным путем. Существует мнение, что доминантный тип наследования свойствен главным образом III и IV типам болезни Штаргардта.
 Позиционным клонированием определен локус вызывающего болезнь гена для болезни Штаргардта, экспрессирующегося в фоторецепторах, который был назван ABCR. Показано, что ABCR идентичен по своей последовательности гену человека RmP.
Позиционным клонированием определен локус вызывающего болезнь гена для болезни Штаргардта, экспрессирующегося в фоторецепторах, который был назван ABCR. Показано, что ABCR идентичен по своей последовательности гену человека RmP.
Белок RmP является интегральным мембранным гликопротеином с молекулярным весом 210 кДа, который локализуется по краю дисков наружных сегментов зрительных клеток. Показано, что RmP относится к суперсемейству ABC-переносчиков АТФ-связывающих кассет, которые стимулируют гидролиз АТФ и влияют на АТФ-зависимое перемещение специфических субстратов через клеточные мембраны.
Выявлено, что гены для нескольких членов суперсемейства АВС-переносчиков вовлечены в развитие ряда наследственных заболеваний сетчатки человека. Так, при аутосомно-доминантном типе наследования болезни Штаргардта показана локализация мутированных генов на хромосомах 13q и 6ql4, а также картирован ген для новой доминантной формы Штаргардт-подобного заболевания сетчатки (возможно, относящегося к типу IV) на хромосоме 4р между маркерами D4S1582 и D4S2397.
Человеческий ген RmP картирован между маркерами D1S424 и D1S236 на хромосоме lp (Ip21-pl3). Там же локализованы гены наиболее распространенной аутосомно-рецессивной формы дистрофии Штаргардта и фундус флавимакулятус, а место гена аутосомно-рецессивной формы пигментного ретинита RP19 определено между маркерами D1S435-D1S236 на хромосоме lp. В исследовании S.M. Azarian и соавт. (1998) установлена полная тонкая интрон-экзонная структура гена ABCR.
С помощью иммунофлюоресцентной микроскопии и вестерн-блоттинг-анализа показано, что ABCR присутствует в фовеальных и перифовеальных колбочках, в связи с чем полагают, что потеря центрального зрения при дистрофии Штаргардта может быть прямым следствием фовеальной колбочковой дегенерации, вызванной мутациями гена ABCR.
Выявлено также, что мутации ABCR имеются в субпопуляции пациентов с неэкссудативной формой макулярной дегенерации, связанной с возрастом (АМД) и колбочко-палочковой дистрофией, что позволяет предполагать наличие генетически обусловленного риска развития АМД у родственников больных с болезнью Штаргардта. Однако это утверждение поддерживают не все исследователи, хотя не подвергается сомнению тот факт, что фенотипические и генотипические проявления болезни Штаргардта и АМД связаны с мутациями гена ABCR.
J.M. Rozet и соавт. (1999), обследуя семейство, имеющее среди своих членов больных и с пигментным ретинитом, и с болезнью Штаргардта, показали, что гетерозиготность гена ABCR приводит к развитию дистрофии Штаргардта, а гомозиготность - к развитию пигментного ретинита.
Таким образом, результаты генетических исследований последних лет свидетельствуют о том, что, несмотря на явные различия в клинической картине пигментного ретинита, болезни Штаргардта, фундус флавимакулятус и АМД, они являются аллельными нарушениями локуса ABCR.
Широкий диапазон фенотипических проявлений дистрофии Штаргардта и возраста выявления клинических признаков (от первой до седьмой декады жизни), наблюдаемых даже в одной семье, делает трудным дифференциальный диагноз и прогноз изменений остроты зрения. Данные ангиографии, анамнез заболевания, сниженные зрительные функции, измененные колбочковые компоненты в ЭРГ, специфика изменений локальной и мультифокальной ЭРГ помогают в постановке диагноза.
Таким образом, в последние годы все большее значение для диагностики придают результатам генетических исследований. Так, G.A. Fishman и соавт. (1999), обследовав большую группу больных с дистрофией Штаргардта и фундус флавимакулятус, имеющих мутации гена ABCR, показали, что вариабельность фенотипических проявлений определенным образом зависит от вариации специфической последовательности аминокислот. По результатам флюоресцентной ангиографии, офтальмоскопии, электроретинографических и периметрических исследований ими было выделено три фенотипа заболевания
- Для одного из этих фенотипов характерно наряду с атрофическими повреждениями макулы появление перифовеально желтовато-белых пятен отсутствие темной сосудистой оболочки и нормальная амплитуда волн ЭРГ. При этом фенотипе установлено изменение последовательности в экзоне 42 гена ABCR, заключающееся в замещении глицина глутамином (Gly]961Glu).
- Другой фенотип отличался темной сосудистой оболочкой и более диффузно разбросанными по глазному дну желтовато-белыми пятнами но замены Glyl961Glu не выявлено.
- При фенотипе с выраженными атрофическими изменениями РПЭ и редуцированными палочковой и колбочковой ЭРГ мутация ABCR найдена только у одного больного из 7.
В связи с тем что мутации ABCR сопровождаются различными фенотипическими проявлениями, полагают, что успехи в идентификации корреляций между специфическими мтациями гена и клиническими фенотипами облегчат консультирование больных и по поводу прогноза остроты зрения.
Все эти исследования направлены не только на раскрытие тонких механизмов генетических заболеваний сетчатки, но и на поиск возможной их терапии.
Клиническая картина
 Поле зрения
Поле зрения
При фундус флавимакулятус поле зрения может быть не изменено, особенно в первые две декады жизни, у всех больных с болезнью Штаргардта выявляют относительные или абсолютные центральные скотомы разной величины в зависимости от распространения процесса в макулярной области.
Цветовое зрение
У большинства пациентов с болезнью Штаргардта I типа отмечается дейтеранопия; при II типе болезни Штаргардта нарушения цветового зрения более выраженные и не поддаются классификации. Вид цветоаномалии, по-видимому, зависит от того, какой тип колбочек преимущественно вовлечен в патологический процесс, поэтому при фундус флавимакулятус цветовое зрение может быть не изменено либо отмечается красно-зеленая дихромазия.
Темновая адаптация
По данным О. Gelisken, J.J. De Jaey (1985), из 43 пациентов с болезнью Штаргардта и фундус флавимакулятус у 4 был повышен конечный порог световой чувствительности, у 10 отсутствовал колбочковый отрезок кривой темновой адаптации.
Пространственная контрастная чувствительность
При дистрофии Штаргардта изменена во всем диапазоне частот со значительным снижением в области средних пространственных частот и полным ее отсутствием в области высоких пространственных частот - паттерн колбочковой дистрофии.
Контрастная чувствительность , on- и off-активность колбочковой системы, оцениваемые по времени сенсомоторной реакции при предъявлении стимула темнее и светлее фона, отсутствуют в центральной области сетчатки с некоторой сохранностью off-чувствительности в зоне 10° от центра.
Электроретинография и электроокулография
 Из электрофизиологических методов электроретинография и электроокулография при диагностике и дифференциальной диагностике заболеваний макулярной области сетчатки являются наиболее информативными.
Из электрофизиологических методов электроретинография и электроокулография при диагностике и дифференциальной диагностике заболеваний макулярной области сетчатки являются наиболее информативными.
По данным литературы, в начальных стадиях дистрофии Штаргардта и фундус флавимакулятус общая, или ганцфельд, ЭРГ нормальна. Однако применение различных методических приемов электроретинографии позволяет оценить топику функциональных нарушений в сетчатке на уровне ее различных слоев и отделов.
Так, при регистрации локальной ЭРГ (ЛЭРГ) с помощью светодиода, вмонтированного в линзу-присоску, биопотенциалы макулярной области субнормальны уже в начальной стадии дистрофии Штаргардта в отличие от нормальных амплитуд ганцфельд-ЭРГ. По мере прогрессирования процесса ЛЭРГ снижается вплоть до полного исчезновения. Другие авторы отмечают также удлинение пиковой латентности и снижение амплитуд локальных фовеальных, ответов; у 64 % больных с фундус флавимакулятус при остроте зрения 20/20 - 20/30.
Применение зональной электроретинографии позволило выявить угнетение реакции наружного слоя сетчатки (фоторецепторов) не только в макулярной зоне, но и в парамакулярном и периферическом отделах в ранних стадиях болезни Штаргардта при сохранности проксимальных слоев сетчатки.
Снижение амплитуд а- и 1 а волн ЭРГ в разных зонах сетчатки (центр, парацентр, периферия) свидетельствует о генерализованном поражении всего фоторецепторного слоя обеих систем (колбочковой и палочковой) уже в первой стадии заболевания. Развитие процесса сопровождается распространением патологических изменений в глубь сетчатки, что выражается в увеличении частоты выявления и степени выраженности изменений всех компонентов ЭРГ.
Однако уже в начальных (I-II) стадиях болезни Штаргардта выявляют большую степень угнетения колбочковых компонентов ЭРГ по сравнению с палочковыми.
По данным P. A. Blacharski (1988), после длительной темновой адаптации (45 мин) у больных с фундус флавимакулатус отмечают большую (на 29 %) степень снижения фотопических компонентов ЭРГ, чем у здоровых лиц. Ответы же скотопической ЭРГ снижаются незначительно, всего на 6-10 %. Согласно сведениям J. B. M. Moloney и соавт. (1983 г.), угентение колбочковой ЭРГ выявляют у 100 % обследованных и снижение палочковой ЭРГ - у 50%.
R. Itabashi и соавт. (1993) представили результаты обследования большой группы больных с болезнью Штаргардта, сравнив степень угнетения различных компонентов ЭРГ.
Согласно классификации, предложенной K.G. Noble и R.E. Сагг (1971), были выделены несколько групп больных по стадиям заболевания: 1-4. Средние амплитуды всех компонентов ЭРГ оказались ниже нормальных значений при более выраженных изменениях колбочковой системы сетчатки. Фотопическая b-волна составляла 57,4 % от нормы, скотопическая b-волна - 77,9 %, ответы на "белый" мелькающий стимул 32 Гц - 78,9 %, а-волна - 87,7 %, b-волна - 95,8 % от нормы. Наибольшее снижение всех компонентов ЭРГ отмечено у больных группы 3.
Временные параметры также были изменены; удлинение пикового времени наиболее значительно для а-волны, особенно у больных группы 3. Для этой стадии характерно также наиболее частое выявление субнормального свето-темнового коэффициента ЭОГ (73,5 %). По мнению авторов, прогноз у больных в группе 3 наиболее неблагоприятен.
Наблюдение за больными на протяжении 7-14 лет позволило проследить динамику электрофизиологических показателей в сопоставлении с клиникой процесса. Более выраженные офтальмоскопические изменения сопровождались снижением как электроретинографических, так и электроокулографических показателей. Эти результаты согласуются с мнением других исследователей, которые на основании электроретинографических и гистологических данных предполагают первоначальное поражение в РПЭ при фундус флавимакулятус и дальнейшее поражение фоторецепторов сетчатки при дистрофии Штаргардта.
В литературе имеются определенные расхождения в результатах электроокулографии. Чаще всего отмечают нормальную или несколько сниженную ЭОГ у большинства больных с фундус флавимакулятус и дистрофией Штаргардта. Однако ряд исследователей отмечают высокий процент субнормальной ЭОГ по величине коэффициента Ардена: у 75-80 % больных ФФ. Следует учитывать, что в большинстве публикаций приведены результаты обследования немногочисленных групп пациентов: от 3 до 29.
G.A. Fishman (1976, 1979) провел корреляцию между стадиями фундус флавимакулятус и результатами ЭОГ. Он показал, что при заболевании I-II стадий у всех обследованных ЭОГ не изменена (28/28), тогда как при III-IV стадиях у 90 % больных она субнормальна. По мнению G.A. Fishman и соавт (1976 1977 1979), лишь в случае поражения патологическим процессом значительной площади сетчатки ЭОГ будет аномальной. Другие исследователи также отмечают отсутствие изменений ЭОГ у подавляющего большинства больных с фундус флавимакулятус. Не исключено что на результаты исследований оказывают влияние различия в методических приемах, несмотря на попытки их стандартизации.
Таким образом, электрофизиологические исследования скорее позволяют выявить наличие и степень выраженности изменений колбочковой и палочковой систем сетчатки, а также оценить состояние РПЭ, чем помогают при дифференциальной диагностике болезни Штаргардта и фундус флавимакулятус.
Дифференциальный диагноз
Клиническая картина при некоторых наследственных заболеваниях может быть схожа с таковой при болезни Штаргардта. К таким заболеваниям относится доминантная прогрессирующая фовеальная дистрофия, колбочко-палочковая и палочко-колбочковая (retinitis pigmentosa) дистрофии, ювенильный ретиношизис. Атрофическая макулярная дегенерация описана при различных спиноцеребральных и церебральных спастических нарушениях, в том числе при олигопонтоцеребральной атрофии. Подобные морфологические находки описаны и при ненаследственных заболеваниях, например при хлорохиновой ретинопатии или глазных проявлениях тяжелого токсикоза беременных.

На основании различий картины глазного дна, возраста, начала заболевания, данных функциональных методов исследования S. Merin (1993) выделил два основных типа болезни Штаргардта.
Болезнь Штаргардта I типа
Этот тип наиболее соответствует первоначально описанной болезни Штаргардта. Это ювенильная наследственная макулодистрофия, клинические проявления которой наблюдаются у детей уже в возрасте 6-12 лет. С одинаковой частотой заболевают мальчики и девочки, наследственная передача осуществляется по аутосомно-рецессивному типу.
Заболевание проявляется билатерально и симметрично. В развитых стадиях фовеальный рефлекс отсутствует. Изменения на уровне пигментного эпителия сетчатки (РПЭ) проявляются в виде скопления в центре коричневатого пигмента, окруженного участками гипер- и депигментации. Клиническая картина напоминает "бычий глаз".
При флюоресцентной ангиографии подтверждают типичный феномен "бычьего глаза". Темный, не пропускающий флюоресцеина центр окружен широким кольцом гипофлюоресцирующих точек, за которым обычно следует другое кольцо гиперпигментации. Такая картина объясняется увеличением количества пигмента в центральной зоне глазного дна, атрофией прилежащих клеток РПЭ и комбинацией атрофии и гипертрофии пигментного эпителия. Отсутствие флюоресцеина в макулярной области называют "молчащей хороидеей" или темной хороидеей и объясняют накоплением кислых мукополисахаридов в РПЭ. По мнению D.A. Klein и А.Е. Krill (1967), феномен "бычьего глаза" выявляют почти у всех больных с болезнью Штаргардта I типа.
По мере прогрессирования заболевания острота зрения снижается, в результате чего развивается слабовидение. Если на ранних этапах болезни ЭРГ и ЭОГ сохраняются нормальными в развитых стадиях снижаются ответы колбочковой системы по данным ЭРГ и становятся умеренно субнормальными показатели ЭОГ. В связи с поражением преимущественно колбочковой системы у больных нарушается и цветовое зрение, чаще по типу дейтеранопии.
При гистологическом исследовании двух глаз больного с типичной болезнью Штаргардта I типа, погибшего в результате автокатастрофы, R.C. Eagl и соавт. (1980) обнаружили значительную вариабельность размеров клеток РПЭ - от 14 до 83 мкм. Крупные клетки РПЭ образовывали гранулярную субстанцию, которая по ультраструктуре, аутофлюоресцентным и гистохимическим свойствам соответствовала патологическому (анормальному) липофусцину. Количество меланина было уменьшено, и меланиновые гранулы были смещены в сторону внутренней части клетки
В более поздних стадиях болезни Штаргардта выявлено исчезновение большей части фоторецепторов и клеток РПЭ из макулярной области сетчатки. При этом часть клеток РПЭ находилась в стадии дегенерации с накоплением липофусцина, по краям участков атрофии наблюдалась гиперплазия клеток РПЭ.
F. Schutt и соавт. (2000) показали, что при заболеваниях сетчатки, связанных с интенсивным накоплением липофусцина, в том числе при болезни Штаргардта, АМД и старении сетчатки, определенную роль в нарушение функции РПЭ вносит ретиноидный флюоресцентный компонент липофусцина А2-Е (N-ретинилиден-N-ретинил-этанол-амин). Он ослабляет деградативную функцию лизосом и увеличивает интрализосомальную рН клеток РПЭ, приводя к потере их мембранной целостности. Кроме лизосомотропических свойств показаны фотореактивные свойства А2-Е, его фототоксичность.
Болезнь Штаргардта II типа
В отличие от I типа, помимо типичных изменений в макулярной области сетчатки, на глазном дне имеются множественные и распространенные пятна ФФ, которые могут достигать экватора. Заболевание начинается несколько позже, хотя это может быть связано с тем, что снижение остроты зрения при II типе болезни Штаргардта происходит медленнее и вследствие этого пациенты позже обращаются к окулисту. В связи с тем, что при болезни Штаргардта II типа отмечается больше изменений, выходящих за границы макулярной области, электрофизиологические данные отличаются от таковых при I типе.
Так, в ЭРГ значительно снижены ответы палочковой системы. Показатели ЭОГ также изменены в большей степени. Наличие в высоком проценте случаев за пределами макулярной области (желтого пятна) желтоватых пятен затрудняет четкое разделение болезни Штаргардта и ФФ.
Фундус флавимакулятус
Как правило, фундус флавимакулятус, или желтопятнистое глазное дно, сочетается с болезнью Штаргардта и как изолированная форма заболевания сетчатки встречается не часто. В типичных ("чистых") случаях у больных практически отсутствуют симптомы заболевания. Острота зрения, цветовое зрение, поле зрения находятся в пределах нормы. Темновая адаптация может быть нормальной или незначительно сниженной. На глазном дне макула и периферия сетчатки без изменений, лишь между фовеа и экватором видны множественные сероватые или желтоватые пятна различной формы: округлые, овальные, удлиненные, в форме запятой или рыбьего хвоста, которые могут сливаться или располагаться отдельно друг от друга, быть мелкими - 200-300 мкм или в 3-5 раз больше. При динамическом наблюдении цвет, форма, размеры этих пятен могут изменяться. Пятна, первоначально желтоватые и четко очерченные, через несколько лет могут стать серыми с нечеткими границами или исчезнуть.
Параллельно этому картина, выявляемая при флюоресцентной ангиографии, становится иной: участки с гиперфлюоресценцией становятся гипофлюоресцирующими. На последующих этапах развития заболевания атрофия РПЭ проявляется как исчезновение отдельных пятен и их замена на нерегулярные участки гипофлюоресценции.
Подобные изменения пятен при фундус флавимакулятус (ФФ) характерны для обоих типов болезни Штаргардта, однако при "чистой форме" ФФ они менее выражены.
Начало заболевания, а скорее всего время его выявления, не зависит от возраста. Предполагается аутосомно-рецессивный тип наследования ФФ, однако в ряде случаев не удается установить наследственную природу данной патологии.